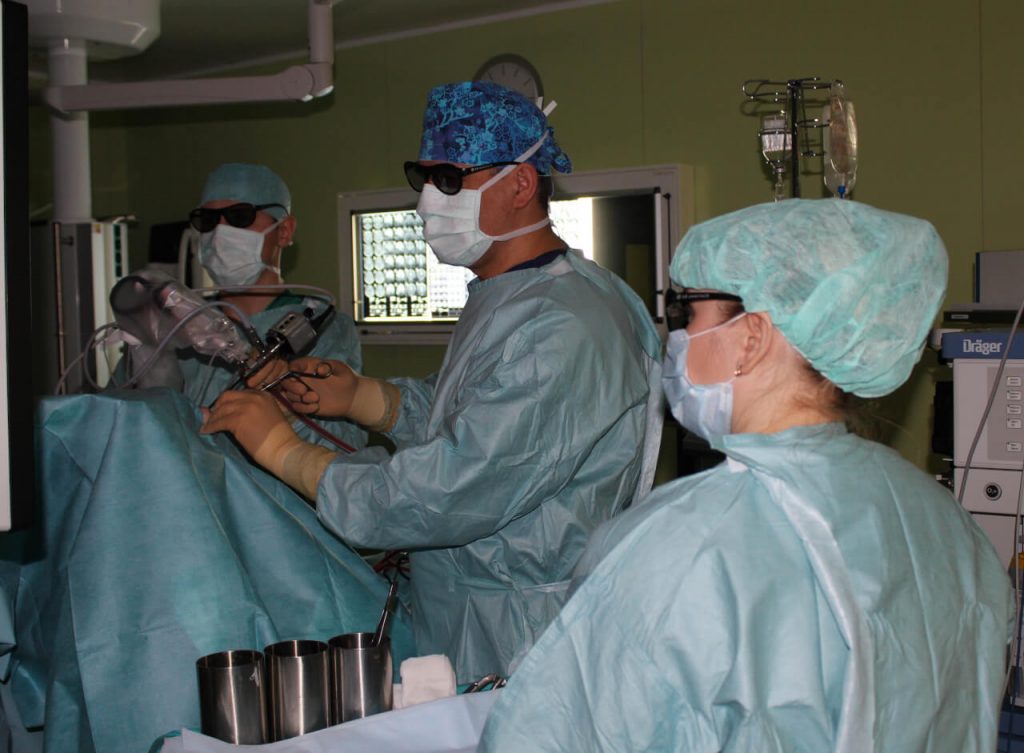
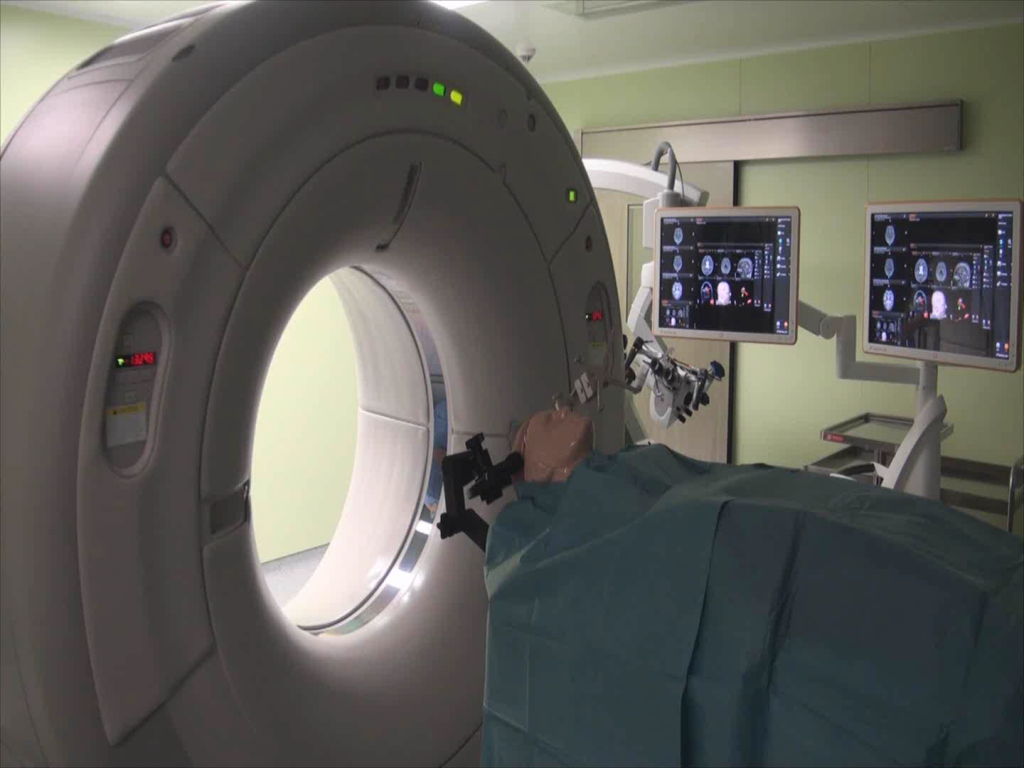
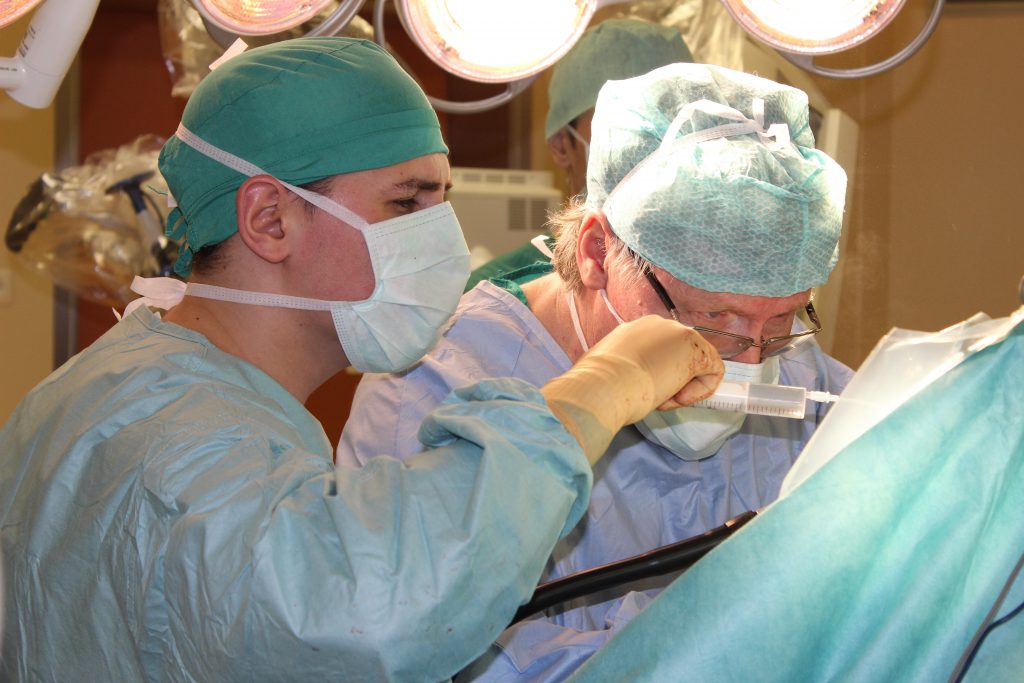
Врач-онколог Федерального центра нейрохирургии в Тюмени рассказывает о причинах возникновения онкологии
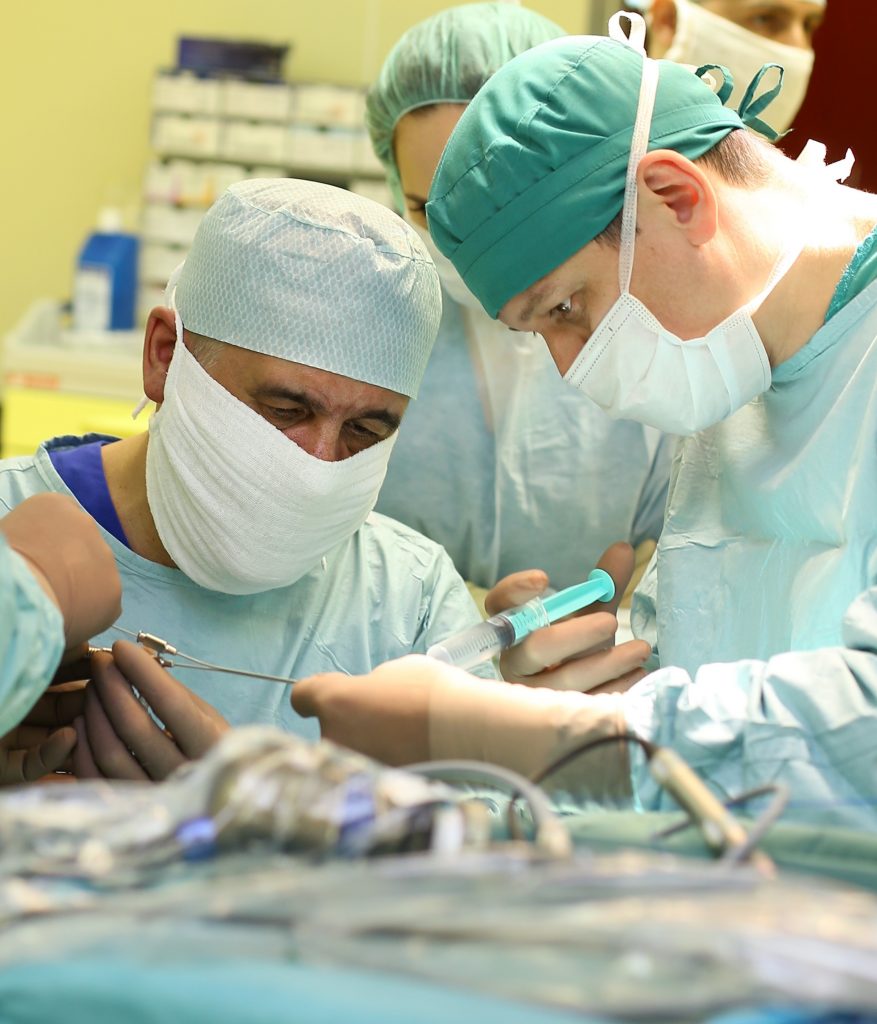
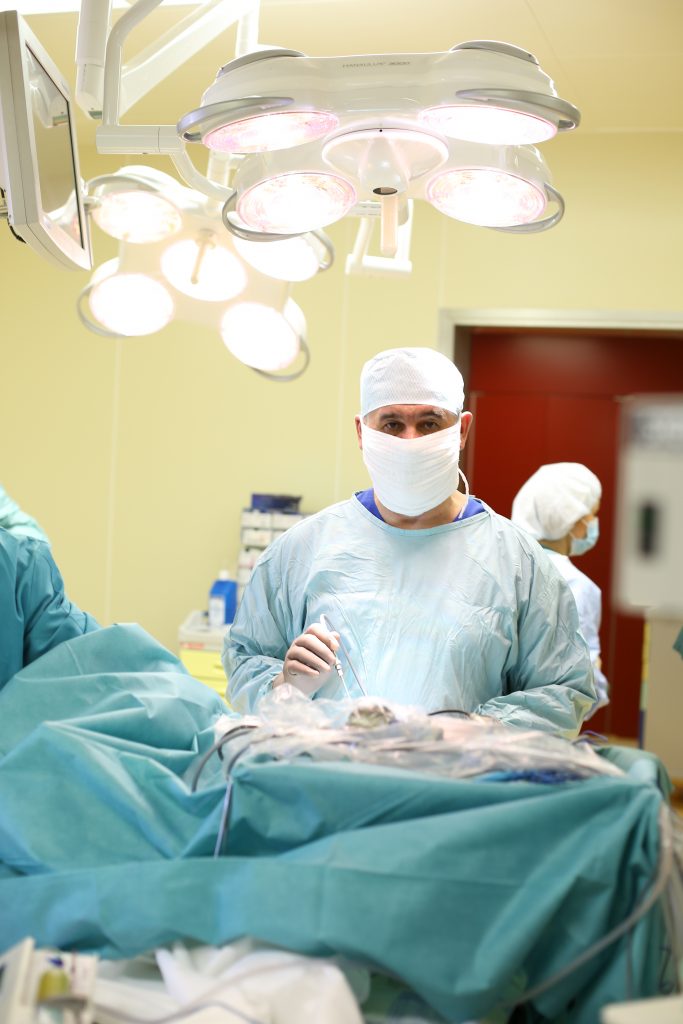
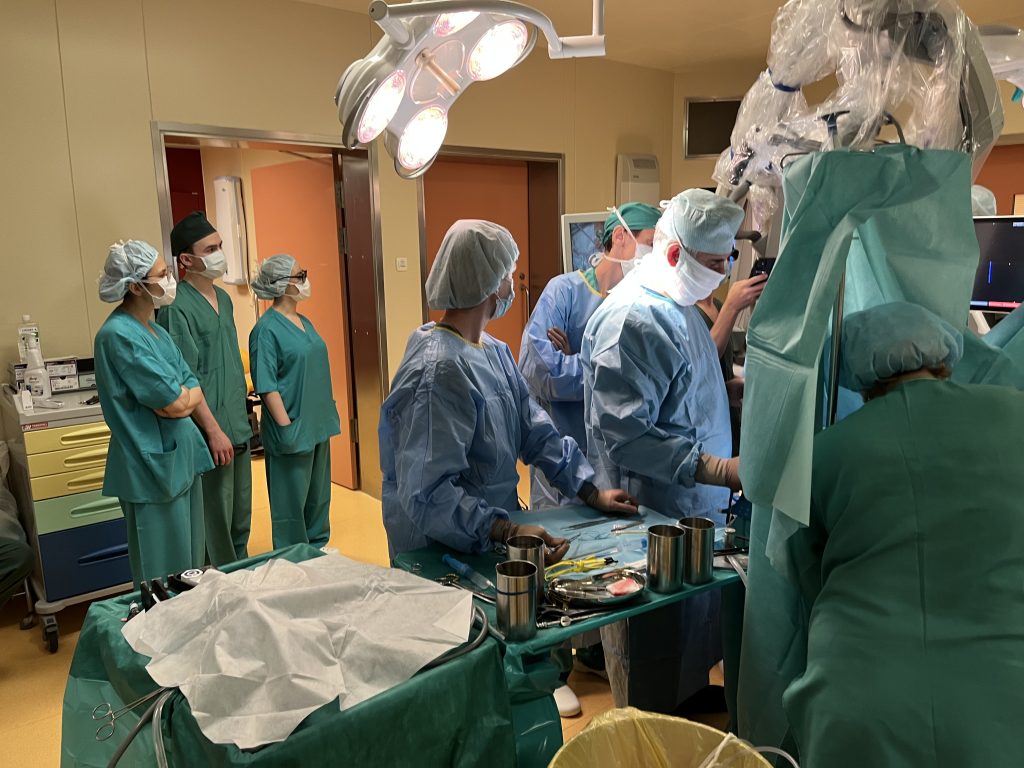
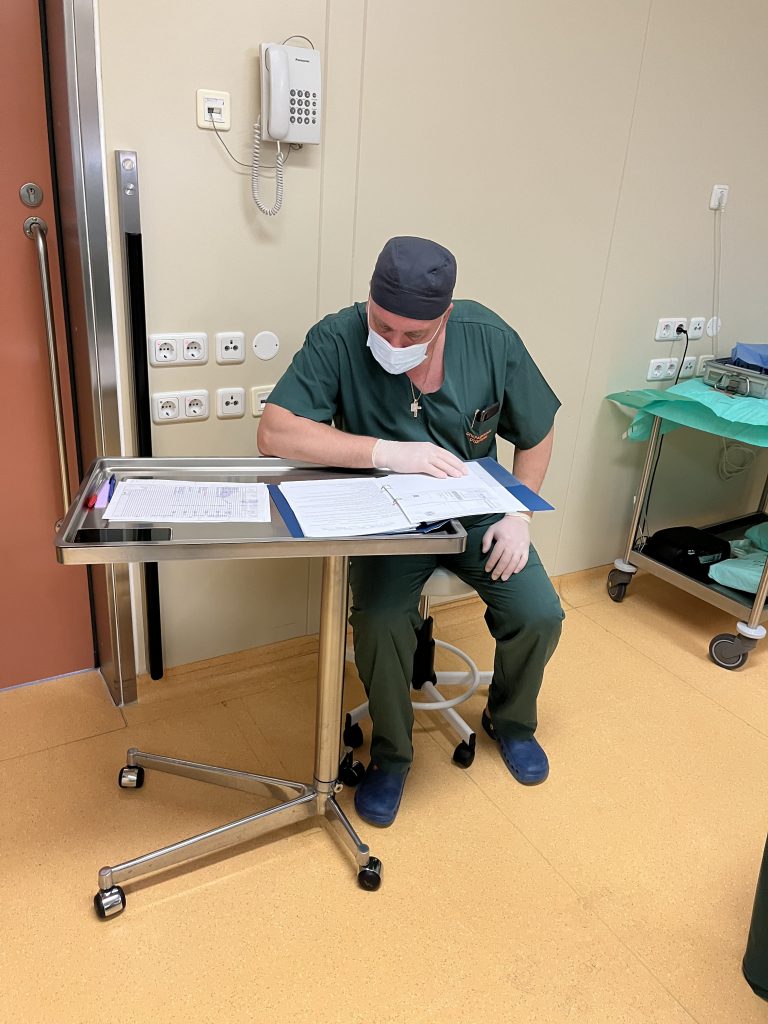
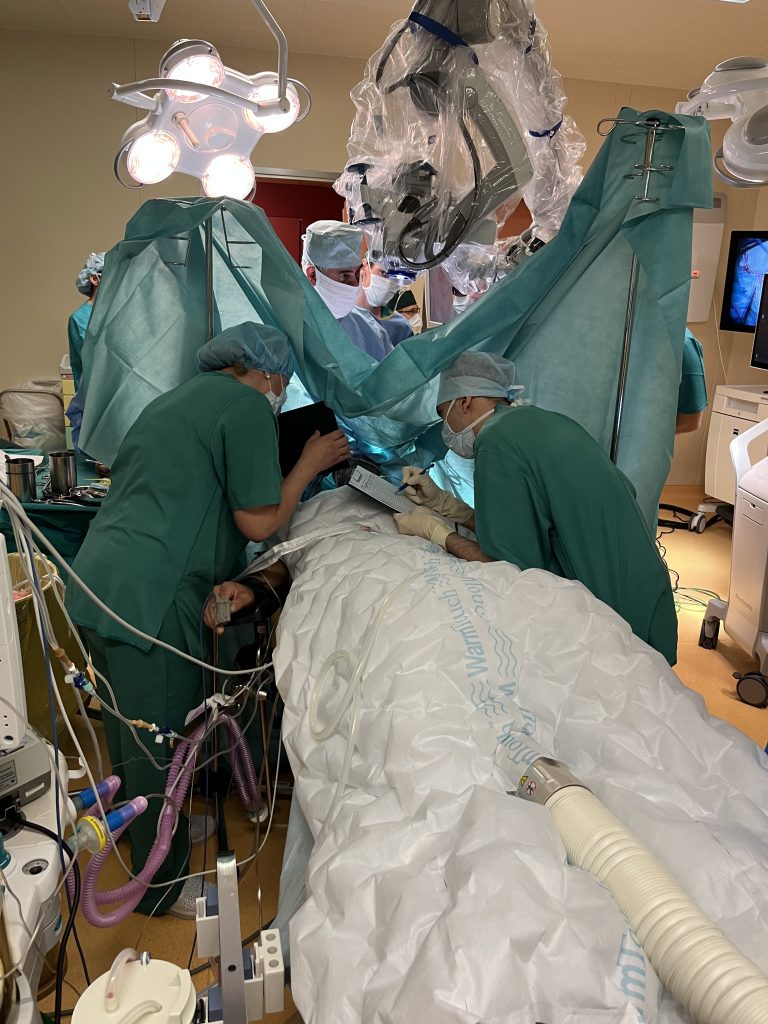
Врач-онколог Федерального центра нейрохирургии Тюмени Станислав Попов более 20 лет помогает больным раком. За годы его работы появились новые лекарства, методы лечения, но главная загадка – причина возникновения онкологии – до сих пор не разгадана. Более того, с годами проблема только усугубляется, а рак молодеет. Свою лепту внесла и пандемия коронавируса.
Что приводит к раку, почему социальные проблемы могут стать одним из факторов возникновения опухоли и какая самая частая жалоба онкобольных. Об это после интервью с врачом центра рассказала в своем в материале журналист издания АИФ tmn.aif.ru.
Читаем — https://tmn.aif.ru/view/health/4816170?key=d85b1ec923a70ee37b4f4aaf71307654